Zusammenfassung
Der Begriff Aortendissektion bezeichnet die Spaltung der Gefäßwand der Aorta
Eine Aortendissektion kann durch ein Trauma (z.B. im Rahmen eines Verkehrsunfalls bei sehr starkem Abbremsen ⟶ Dezelerationstrauma), aber auch durch Erkrankungen wie arterielle Hypertonie, Arteriosklerose
Eine Aortendissektion kann als akut (<14 Tage), subakut (15-90 Tage) oder chronisch (>90 Tage) klassifiziert werden.
Weiterhin wird die Aortendissektion nach ihrer Lokalisation gemäß der Stanford-Klassifikation (oder der DeBakey-Klassifikation) unterteilt:

MerkeStanford A: Ascending Aorta
Stanford B: Begins behind brachicephalic vessels
Epidemiologie
- Häufigkeit:
- Inzidenz: ca. 3–6 Fälle pro 100.000 Einwohner:innen pro Jahr
- Typ-A-Dissektion (Stanford-Klassifikation) häufiger als Typ-B-Dissektion
- Alter:
- Gipfel 50-70 Jahre
- Jüngere Patient:innen betroffen bei genetischen Prädispositionen (z. B. Marfan-Syndrom → Gipfel 30. Lebensjahr, Ehlers-Danlos-Syndrom)
- Geschlechterverteilung:
- Männer häufiger betroffen (ca. 3:1 im Vergleich zu Frauen)
- Lokalisation:
- Typ A: ca. 71%
- Typ B: ca. 29%
Pathophysiologie

Eine Aortendissektion entsteht durch einen Einriss der Intima, wodurch Blut in die Media eindringt und ein falsches Lumen bildet. Der Scherkräfte-bedingte Riss wird durch arterielle Hypertonie
Ursachen/Risikofaktoren
Die Aortendissektion wird durch eine strukturelle Schwächung der Aortenwand in Kombination mit hämodynamischen Kräften begünstigt. Der wichtigste prädisponierende Faktor ist eine arterielle Hypertonie
Hauptrisikofaktoren:
- Arterielle Hypertonie
(häufigste Ursache, >70 % der Fälle) - Aortenaneurysma
- Bindegewebserkrankungen
: - Marfan-Syndrom (Mutation des Fibrillin-1-Gens)
- Ehlers-Danlos-Syndrom vom vaskulären Typ (Defekte in Kollagen Typ III)
- Loeys-Dietz-Syndrom
- Degenerative Veränderungen der Media:
- Zystische Medianekrose (v. a. bei älteren Patient:innen und Hypertonie
) - Elastin- und Kollagenabbau
- Zystische Medianekrose (v. a. bei älteren Patient:innen und Hypertonie
- Atherosklerose
: - Verdünnung und Infiltration der Gefäßwand
- Erhöhtes Risiko für Ulzera und Plaquerupturen
- Angeborene Herzfehler:
- Bikuspidale Aortenklappe
- Aortenisthmusstenose
- Iatrogene Ursachen:
- Aorteninterventionen (z. B. Katheteruntersuchungen, Operationen)
- Traumatische Ursachen:
- Dezelerationstrauma (z. B. durch Verkehrsunfälle mit abruptem Abbremsen)
- Direkte Gefäßverletzungen
- Schwangerschaft:
- Besondere Risikoerhöhung im dritten Trimester durch hormoninduzierte Veränderungen der Media
- Zusätzliche hämodynamische Belastung
- Familiäre Formen des thorakalen Aortenaneurysmas und der Aortendissektion → positive Familienanamnese bei erstgradigen Verwandten
- Drogenkonsum (z. B. Kokain
oder Amphetamine durch plötzliche hypertensive Peaks) - Entzündliche Erkrankungen (z. B. Riesenzellarteriitis oder Syphilis-Aortitis, Takayasu-Arteriitis), die die Gefäßwand schwächen und das Risiko einer Dissektion erhöhen
Klassifikation
Die Stanford- und De-Bakey-Klassifikationen sind zwei Klassifikationen zur Einteilung von Aortendissektionen. Diese Klassifikationen ordnen die Lokalisation der Aortendissektion ein, was für die Planung der Therapie entscheidend ist.
Stanford-Klassifikation:
Die Stanford-Klassifikation teilt Aortendissektionen basierend auf der Beteiligung der Aorta ascendens
- Stanford Typ A: Hierbei ist die Aorta ascendens
betroffen. Diese Form ist die gefährlichere der beiden Typen, da sie häufig schwerwiegende Komplikationen wie eine Aortenklappeninsuffizienz , Herzbeuteltamponade oder einen Myokardinfarkt verursacht. Der Typ A erfordert in der Regel eine sofortige chirurgische Intervention - Stanford Typ B: Hierbei ist die Aorta ascendens
nicht betroffen, die Dissektion beginnt distal der linken Arteria subclavia . Der Typ B kann oft konservativ behandelt werden, es sei denn, es treten Komplikationen wie Rissbildung, Durchblutungsstörungen der Organe oder ein Fortschreiten der Dissektion auf
MerkeStanford A: Ascending Aorta
Stanford B: Begins behind brachicephalic vessels
De-Bakey-Klassifikation:
Die De-Bakey-Klassifikation basiert auf dem Ursprung und der Ausdehnung der Dissektion:
- De-Bakey Typ I: Die Dissektion beginnt in der Aorta ascendens
und erstreckt sich sowohl über den Aortenbogen als auch über die absteigende Aorta . Diese Art ist besonders schwerwiegend und oft tödlich ohne rechtzeitige chirurgische Intervention - De-Bakey Typ II: Die Dissektion ist auf die Aorta ascendens
beschränkt und betrifft den Aortenbogen oder die absteigende Aorta nicht. Auch hier ist eine chirurgische Behandlung in der Regel erforderlich - De-Bakey Typ III: Die Dissektion beginnt in der absteigenden Aorta
distal der linken Arteria subclavia

Akutes Aortensyndrom (AAS):
Das akute Aortensyndrom (AAS) umfasst eine Gruppe lebensbedrohlicher Erkrankungen der Aortenwand, die eine ähnliche Pathophysiologie und Symptomatik aufweisen. Es handelt sich um eine Notfallsituation, die eine schnelle Diagnostik und Therapie erfordert.
Hauptformen des akuten Aortensyndroms:
- Aortendissektion:
- Intimaeinriss mit Einblutung in die Media → Bildung eines falschen Lumens
- Intramurales Hämatom (IMH):
- Blutung innerhalb der Media ohne Intimariss
- Kann in eine Aortendissektion übergehen
- Ähnliche Klinik wie die klassische Dissektion
- Penetrierendes Aortenulkus (PAU):
- Atherosklerotisches Ulkus durchbricht die Intima → Einblutung in die Media
- Prädisposition: Schwerwiegende Atherosklerose
- Kann zur Dissektion oder Ruptur fortschreiten
- Traumatische Aortenverletzung:
- Meist durch Hochgeschwindigkeitstraumata (z. B. Verkehrsunfälle)
- Iatrogene Aortenverletzung (z.B. durch Katheterintervention)
- Häufig betroffene Stelle: Aortenisthmus (Übergang Aortenbogen
→ Aorta descendens )
Klinik
Die Symptomatik einer Aortendissektion ist hochvariabel, hängt von der Lokalisation und Ausdehnung der Dissektion ab und kann unspezifisch sein. Typisch ist ein plötzlich einsetzender, starker Schmerz, jedoch können auch ischämische Komplikationen durch die Beteiligung abgehender Gefäße im Vordergrund stehen.
Leitsymptom: Schmerz
- Charakter:
- Plötzlich einschießend, oft als reißend oder zerreißend beschrieben
- “Stärkster je erlebter Schmerz”
- Lokalisation:
- Aorta ascendens
(Stanford Typ A)/thorakale Dissektion: Brustschmerz, retrosternal - Ausstrahlung: eher Interskapular
- Aorta descendens
(Stanford Typ B)/abdominelle Dissektion: Rücken- oder Flankenschmerz - Ausstrahlung: eher in den Bauch oder in die Beine bei distaler Ausbreitung
- Aorta ascendens
MerkeBei einer Aortendissektion kann es zu sehr variablen Symptomen kommen. Häufig wird der Schmerz als sehr schmerzhaft und schneidend oder reißend ("wie ein Axthieb") beschrieben.
Weitere Symptome je nach betroffener Aortenregion:
- Neurologische Symptome:
- Synkope
- Schlaganfall
-Symptomatik (bei Beteiligung der A. carotis) - Querschnittssyndrom (durch Ischämie des Rückenmarks)
- Synkope
- Kardiovaskuläre Symptome:
- Symptome einer akuten Herzinsuffizienz
, Perikardtamponade , akuten Aortenklappeninsuffizienz - Pulsdefizite
: Unterschiedliche Blutdruckwerte an den Armen (bei einer Subclavia-Beteiligung)
- Symptome einer akuten Herzinsuffizienz
- Ischämiesymptome durch Gefäßverschlüsse:
- Koronararterien
(besonders RCA ): Akutes Koronarsyndrom - Abdominale Organe: Akutes Abdomen
(bei Mesenterialischämie) - Nierenarterien
: Anurie , Nierenversagen - Extremitäten: Akute Beinischämie mit Schmerzen, Blässe und Pulslosigkeit
- Koronararterien
- Schock
und Kreislaufversagen bei Ruptur mit massiver Blutung in Perikard, Pleura oder Retroperitoneum
Die klinische Präsentation ist oft unspezifisch, weshalb eine hohe diagnostische Wachsamkeit erforderlich ist, insbesondere bei Patient:innen mit plötzlichem Schmerz, neurologischen Ausfällen oder hypoperfusionsbedingten Symptomen.
Diagnostik
Anamnese
- S – Symptome:
- Beginn des Schmerzes (akut)
- Schmerzcharakter (reißend, schneidend)
- Schmerzlokalisation und Ausstrahlung (Thorax
, zwischen den Schulterblättern , Rücken, Abdomen, Extremitäten) - Je nach Komplikation: Schocksymptomatik, Angina pectoris
, Symptome einer Perikardtamponade , Symptome einer akuten Herzinsuffizienz (Dyspnoe), fokal-neurologisches Defizit (Synkope , Sehstörungen, Lähmungen), Übelkeit, Erbrechen bei Organischämie, Oligo-/Anurie (Nierenarterienbeteiligung), Extremitätenischämie (pulslos, blass , schmerzhaft) etc.
- A – Allergien:
- Medikamentenallergien (z. B. Analgetika, Kontrastmittel)
- M – Medikamente:
- Einnahme von Antihypertensiva
, Thrombozytenaggregationshemmern oder Antikoagulantien - P – Patientengeschichte/Vorerkrankungen:
- Vorbestehende arterielle Hypertonie
- Bekannte Aneurysmen oder andere Gefäßerkrankungen
- Diagnostizierte Bindegewebserkrankungen
(Marfan-Syndrom, Ehlers-Danlos-Syndrom, Loeys-Dietz-Syndrom) - Kardiale Erkrankungen (z. B. bikuspide Aortenklappe
) - Frühere Eingriffe an Aorta
oder Herz (Operationen, Katheteruntersuchungen)
- Vorbestehende arterielle Hypertonie
- L – Letzte Nahrungsaufnahme:
- Letzte Mahlzeit (vor allem relevant im Hinblick auf eine eventuell notwendige OP)
- E – Ereignisse vor Symptombeginn:
- Körperliche Belastung oder Anstrengung unmittelbar zuvor
- Trauma (z. B. Dezelerationstrauma, Verkehrsunfall)
- Drogenkonsum (insbesondere Kokain
oder Amphetamine)
- R – Risikofaktoren:
- Bekannte Bindegewebserkrankungen
in der Familie - Familiäre Formen des thorakalen Aortenaneurysmas und der Aortendissektion → positive Familienanamnese bei erstgradigen Verwandten
- Schwangerschaft (3. Trimester und peripartal erhöhtes Risiko)
- Rauchen, Hyperlipidämie
, Diabetes mellitus - Chronischer Stress
- Unzureichend eingestellte arterielle Hypertonie
- Bekannte Bindegewebserkrankungen
Körperliche Untersuchung
- Erfassung der Vitalparameter
- Hinweise auf Schock
? - Blutdruckdifferenz zwischen den Armen bei einer Verlegung der A. subclavia
sinistra oder des Truncus brachiocephalicus - Einseitiges Pulsdefizit
- Hinweise auf Schock
- Akute fokal-neurologische Defizite
(z. B. Hemiparese bei A. carotis-Beteiligung) - Auskultation: Neues diastolisches Herzgeräusch → Hinweis auf akute Aortenklappeninsuffizienz
- Gestaute Halsvenen (Hinweis für eine Perikardtamponade
oder Herzinsuffizienz )
Labor
- Blutgasanalyse
: unmittelbare Einschätzung des Hb -Wertes und des Laktats - D-Dimere
: bei uneindeutiger Symptomatik zum Ausschluss einer Aortendissektion (negative D-Dimere schließen eine Aortendissektion nahezu sicher aus – sehr sensitiv, jedoch sehr unspezifisch) - Blutbild
: Hb -Wert bei Blutung, Leukozytose als Hinweis für Infekt - Identifikation von Komplikationen oder Differenzialdiagnosen: Kreatinkinase
, Troponin , Kreatinin , ALT , AST , Laktat, LDH , CRP , Glucose - Troponin
↑: Bei Myokardischämie durch Koronararterienbeteiligung - Nierenwerte
↑ (Kreatinin , Harnstoff ): Zeichen einer Nierenarterienbeteiligung - Laktatwert ↑: Schock
, Mesenterialischämie, periphere Ischämie - ALT
, AST ↑: Hinweise für eine Leberischämie
- Troponin
Apparative Diagnostik
- 12-Kanal-EKG
: zum Ausschluss eines STEMIs
CT
- Schnellste und sensitivste Methode → Goldstandard bei hämodynamisch stabilen Patient:innen
- Darstellung von echtem und falschem Lumen, Einriss der Intima, Dilatationen und Vaskularisation der Organabgänge
- Darstellung der Dissektionsmembran und möglicher Verschlüsse der Aortenäste
- Beurteilung der Ausdehnung
- Identifikation möglicher Komplikationen (z.B. Blutungen, Perikardtamponade
) - Ggf. Darstellung eines Aortenulkus oder eines intramuralen Hämatoms
Transösophageale Echokardiographie
- Indikation: Instabile Patient:innen, OP-Vorbereitung
- Vorteile: Bettseitige Untersuchung möglich, hohe Sensitivität
für proximale Dissektionen (Stanford Typ A) - Nachteile: Eingeschränkte Darstellbarkeit der distalen Aorta
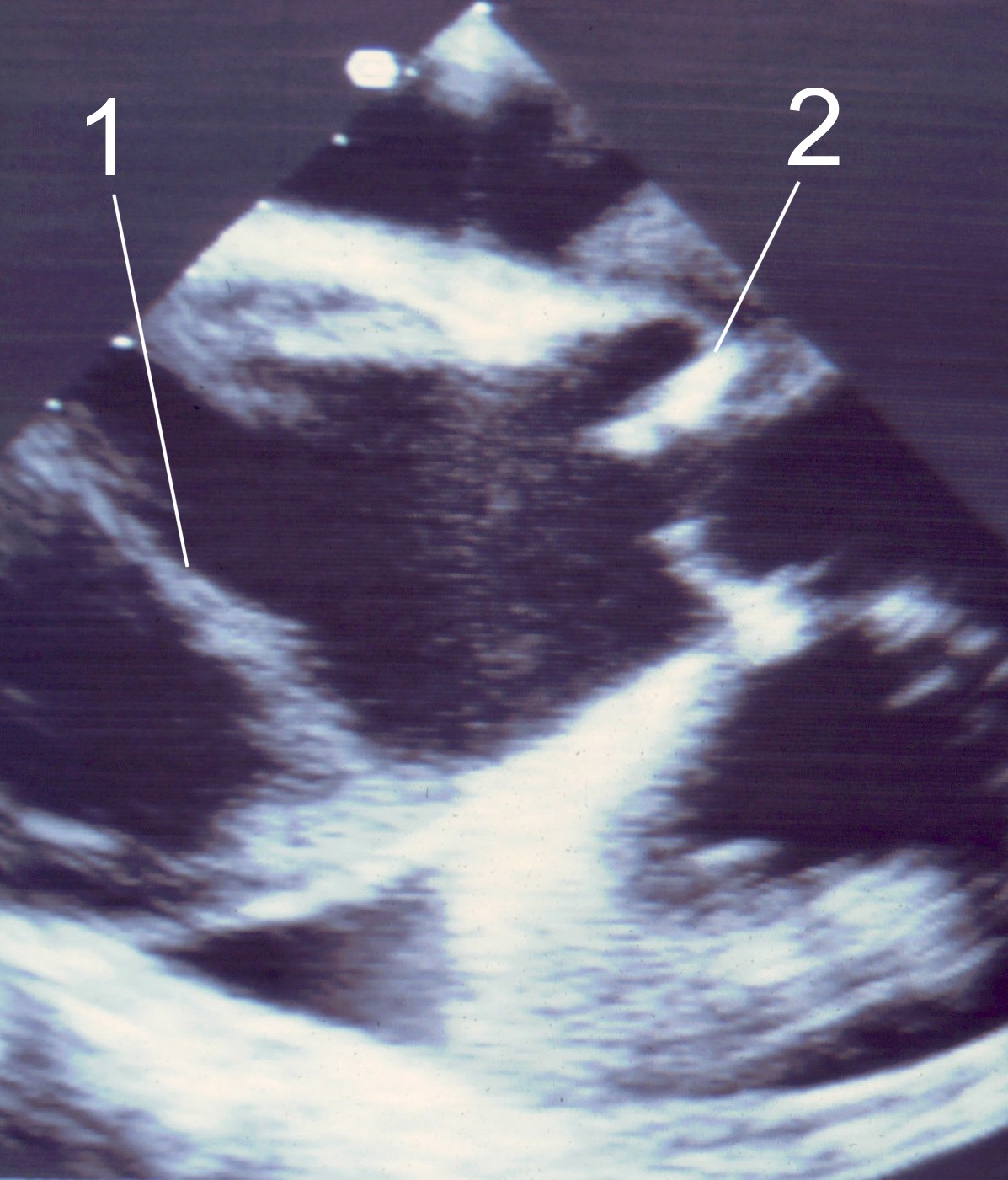
AoDiss TEE BBild.jpg, https://commons.wikimedia.org/wiki/File:AoDiss_TEE_BBild.jpg, J. Heuser JHeuser, CC BY-SA 3.0, http://creativecommons.org/licenses/by-sa/3.0/, via Wikimedia Commons
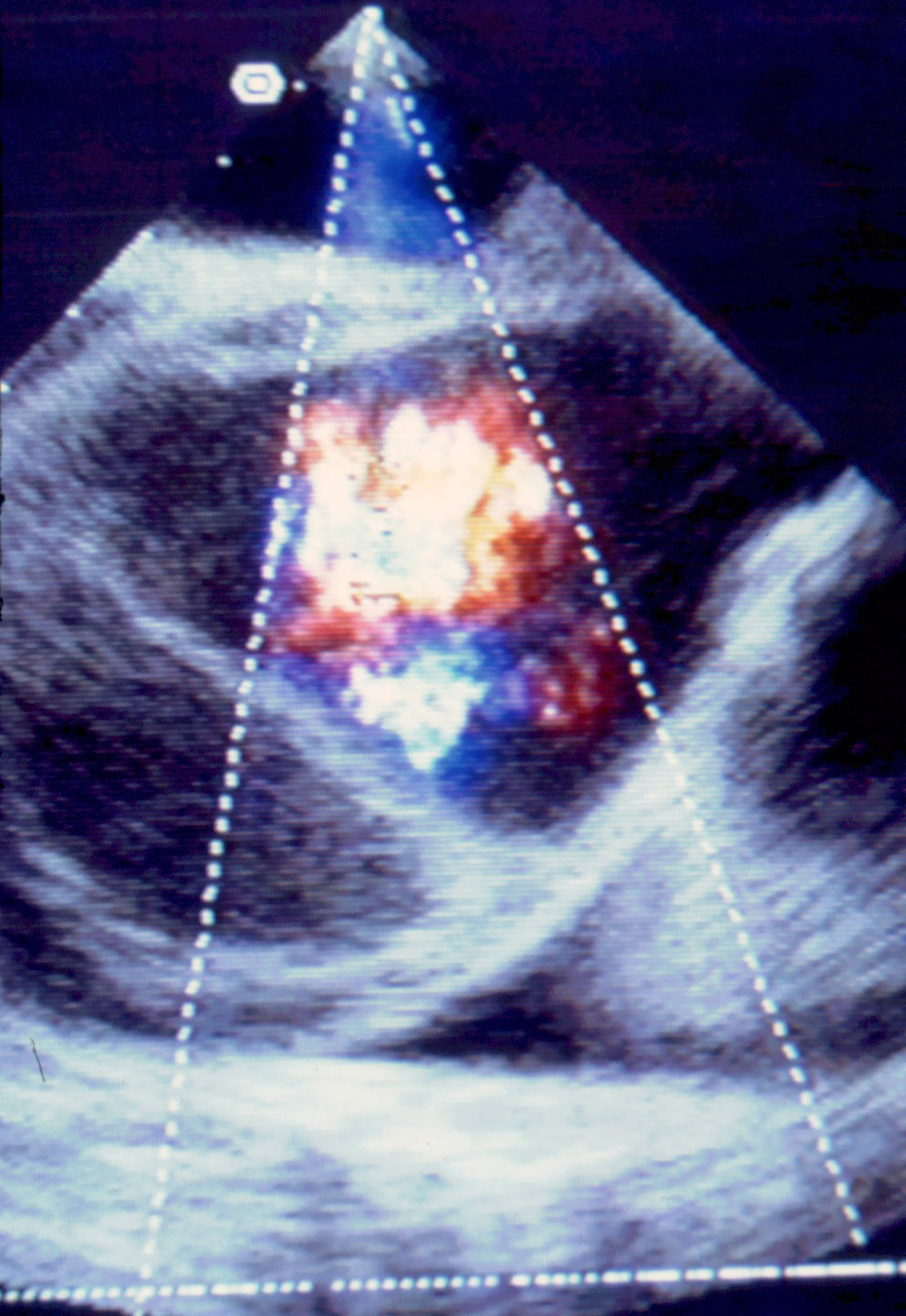
AoDiss TEE color.jpg, https://commons.wikimedia.org/wiki/File:AoDiss_TEE_color.jpg, J. Heuser JHeuser, CC BY-SA 3.0, http://creativecommons.org/licenses/by-sa/3.0/, via Wikimedia Commons
- Transthorakale Echokardiographie
(TTE ): - Limitiert, aber kann eine Aortenklappeninsuffizienz
oder Perikardtamponade detektieren und die Aortenwurzel darstellen
- Limitiert, aber kann eine Aortenklappeninsuffizienz
- Magnetresonanzangiographie (MRA
): - Sehr gute Bildqualität, aber zeitaufwändig → nicht für Notfälle geeignet
- Sonographie des Abdomens: Beurteilung der abdominellen Aorta
- Röntgen-Thorax
: Mediastinalverbreiterung, Doppelkontur der Aorta etc.

JasonRobertYoungMD, CC BY-SA 4.0, https://creativecommons.org/licenses/by-sa/4.0, via Wikimedia Commons
AchtungInstabile Patient:innen oder Hochrisikopatient:innen sollten eine CT
-Angiographie und/oder ein TEE erhalten. Bei einer Aortendissektion Stanford Typ A ist in der Regel eine Notfall-OP notwendig. Bei stabilen Patient:innen mit einer geringen Wahrscheinlichkeit für eine Aortendissektion sollte eine Ausschlussdiagnostik mittels D-Dimeren, TTE
und Röntgen-Thorax erfolgen. Die Wahrscheinlichkeit für eine Aortendissektion kann mittels des Aortendissektion-Risikoscores abgeschätzt werden: https://www.ahajournals.org/doi/10.1161/CIRCULATIONAHA.110.988568
Differenzialdiagnosen
- Akutes Koronarsyndrom
(EKG, Troponin ) - Lungenarterienembolie
(D-Dimere , CT -Angiographie) - Spannungspneumothorax
(klinische Untersuchung, Röntgen-Thorax ) - Ösophagusruptur (Boerhaave-Syndrom
) (Röntgen, Ösophagographie)
Therapie
Die Therapie der Aortendissektion richtet sich nach der Lokalisation (Stanford-Klassifikation), dem klinischen Zustand des/der Patient:in sowie möglichen Komplikationen. Während eine Stanford-Typ-A-Dissektion immer eine sofortige chirurgische Therapie erfordert, wird eine Stanford-Typ-B-Dissektion primär konservativ behandelt, sofern keine Komplikationen auftreten.
Notfallmaßnahmen
- Umgehende Information der Herz-/Gefäßchirurgie
- Engmaschiges hämodynamisches Monitoring
: z.B. arterieller Gefäßzugang - Konsequente Blutdrucksenkung auf ca. 100-120/80 mmHg
- Medikamente: β-Blocker (z. B. Metoprolol
) + ggf. ACE-Hemmer (Ramipril) und/oder Vasodilatatoren (Urapidil )
- Medikamente: β-Blocker (z. B. Metoprolol
- Einstellung der Herzfrequenz
auf ca. 60 Schläge pro Minute (zur Reduktion der Scherkräfte) - bevorzugt mittels Betablockern (z.B. Metoprolol - Schmerztherapie und Stressreduktion: Opioide
z.B. Morphin - Anlage großlumiger Gefäßzugänge
- Vermeidung von körperlicher Belastung und Agitation
- Regelmäßige Ableitung eines 12-Kanal-EKGs
und Bestimmung des Troponin -Wertes zum Ausschluss eines Myokardinfarktes
Instabile Patient:innen oder Patient:innen mit hohem Risiko:
- Atemwegssicherung
- Erweitertes hämodynamisches Monitoring
: z.B. invasive arterielle Blutdruckmessung und Anlage eines ZVK - Sofortige CT-Angiographie/transösophageale Echokardiographie
- Bei Aortendissektion Stanford Typ A, Koronarinsuffizienz, Aorteninsuffizienz
, komplizierter Aortendissektion Stanford Typ B: Notfall-Operation - Bei einer unkomplizierten Aortendissektion Stanford Typ B: Endovaskuläre Aortenreparatur
(EVAR )
Stabile Patient:innen mit geringem Risiko:
- D-Dimere
, transthorakale Echokardiographie , Röntgen-Thorax - Bei positiven Befunden: CT-Angiographie/transösophageale Echokardiographie
/MRT - Bei chronischer, asymptomatischer Aortendissektion:
- Aortendissektion Stanford Typ A: bevorzugt elektive operative Versorgung
- Aortendissektion Stanford Typ B: bevorzugt elektive interventionelle Versorgung
- In Einzelfällen auch konservative Therapie möglich: konsequente Blutdruckeinstellung und Optimierung der Risikofaktoren (z.B. Behandlung einer Dyslipidämie, Einstellung eines Diabetes mellitus
)
- In Einzelfällen auch konservative Therapie möglich: konsequente Blutdruckeinstellung und Optimierung der Risikofaktoren (z.B. Behandlung einer Dyslipidämie, Einstellung eines Diabetes mellitus
Konservative und chirurgische Therapie
Stanford Typ A (Aorta ascendens
- Unbehandelt besteht eine sehr hohe Letalität → zeitnahe operative Versorgung
- Weitere Indikationen für eine Notfall-Operation: Koronarinsuffizienz, Aortenklappeninsuffizienz

Originalabbildung von Servier Medical Art by Servier (https://smart.servier.com/), lizenziert unter einer Creative Commons Attribution 4.0. Diese Abbildung ist ein Derivat der genannten Originalabbildung. Es wurden die Markierungen und die Beschriftungen ergänzt.
- Notfalloperation → Offene chirurgische Versorgung:
- Operation unter Anwendung einer Herz-Lungen-Maschine
- Anlage einer Liquordrainage (Minderperfusion kann zu Ödem
führen → Druckentlastung des Rückenmarks und Verbesserung der Perfusion) - Resektion des Dissektionssegments
- Rekonstruktion mit Gefäßprothese
- Ersatz der Aortenklappe, falls notwendig
- Eventuell Reimplantation der Koronararterien
- Operation unter Anwendung einer Herz-Lungen-Maschine
- Bei chronischer, asymptomatischer Aortendissektion Stanford Typ A: bevorzugt elektive operative Versorgung
AchtungEine Aortendissektion Stanford Typ A muss meistens notfallmäßig operativ versorgt werden! Wenn eine Aortendissektion im Bereich der Aorta ascendens
nachgewiesen wird, sollte eine weitere Diagnostik die Operation nicht verzögern.
Stanford Typ B (nur Aorta descendens
- Konservative Therapie:
- Indikationen:
- Akute Aortendissektion Stanford Typ B ohne Komplikationen und keinen oder nur leichten Symptomen
- Chronische, asymptomatische Aortendissektion Stanford Typ B
- Medikamentöse Blutdruck- und Herzfrequenzkontrolle:
- Blutdruckeinstellung auf unter 130/80 mmHg mit ß-Blockern, ggf. ACE-Hemmern, ggf. Vasodilatatoren
- Regelmäßige Kontrollen
- Blutdruckeinstellung auf unter 130/80 mmHg mit ß-Blockern, ggf. ACE-Hemmern, ggf. Vasodilatatoren
- Behandlung einer Dyslipidämie
- Behandlung eines Diabetes mellitus
- Ernährungsumstellung
, Nikotinkarenz - Bei Schmerzen oder Progredienz: interventionelle Versorgung
- Indikationen:
- Endovaskuläre Therapie:
- Indikationen:
- Komplizierte Dissektion: Aortendurchmesser >60 mm, schnelle Zunahme des Aortendurchmessers, Rupturgefahr, Organischämie, Extremitätenischämie, retograde Ausdehnung oder progredienter Erweiterung
- Nicht beherrschbare Hypertonie
oder Schmerzen trotz optimaler medikamentöser Therapie - Vor und nach der Dissektion sollte eine Landezone (gesunde Aorta
) von mindestens 2 cm sein - Bei Nicht-Durchführbarkeit einer endovaskulären Intervention sollte eine Operation erwogen werden
- Verfahren:
- Ein Stentgraft wird über femorale Zugänge (perkutane Punktion oder chirurgische Freilegung) in die Aorta
eingebracht - Der Stentgraft wird an der gesunden Gefäßwand fixiert und schließt die Dissektion aus dem Blutstrom aus
- Ggf. Anlage einer Liquordrainage (Minderperfusion kann zu Ödem
führen → Druckentlastung des Rückenmarks und Verbesserung der Perfusion) - Bei einer thorakalen Aortendissektion erfolgt eine Thoracic Endovascular Aortic Repair
(TEVAR ) - Bei einer abdominellen Aortendissektion erfolgt eine Endovascular Aneurysm Repair
(EVAR )
- Ein Stentgraft wird über femorale Zugänge (perkutane Punktion oder chirurgische Freilegung) in die Aorta
- Indikationen:
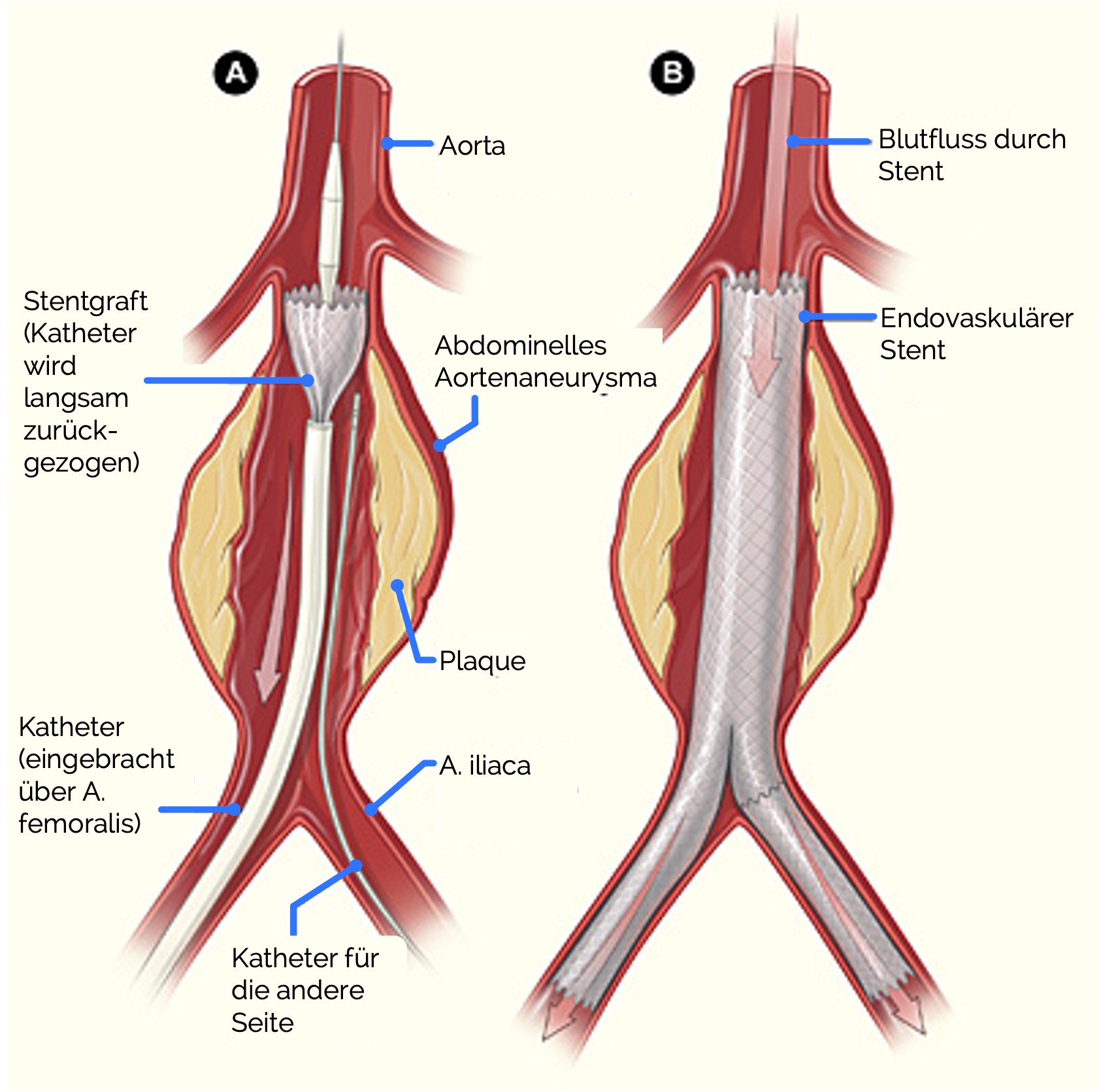
Aneurysm endovascular, https://commons.wikimedia.org/wiki/File:Aneurysm_endovascular.jpg, National Institutes of Health, Public domain, https://creativecommons.org/publicdomain/mark/1.0/deed.en, via Wikimedia Commons. Diese Abbildung ist ein Derivat der genannten Originalabbildung. Es wurden die Markierungen ersetzt und die Beschriftungen übersetzt und teilweise geändert.
AchtungEine Aortendissektion Stanford Typ B kann meistens interventionell mittels einer EVAR
oder sogar konservativ versorgt werden.
TippEine EVAR
und TEVAR ist nur möglich, wenn die anatomischen Gegebenheiten geeignet sind. Nach einer EVAR und TEVAR ist eine lebenslange Nachsorge mit einer regelmäßigen Bildgebung notwendig. Bei der Auswahl des Operationsverfahrens sollte daher auch die Compliance des/der Patient:in berücksichtigt werden.
3. Langfristige Nachsorge
- Lebenslange Blutdruckkontrolle (Zielwert: 120/80 mmHg)
- Regelmäßige Bildgebung (CT-/MR-Angiographie zur Kontrolle des Aortendurchmessers)
- Meiden von schwerem Heben oder körperlicher Anstrengung
- Strenge Kontrolle von kardiovaskulären Risikofaktoren (Lipidsenkung, Nikotinkarenz)
Komplikationen
Aortenruptur
Die Ruptur ist die schwerwiegendste Komplikation einer Aortendissektion und stellt einen chirurgischen Notfall dar.
Klinische Zeichen einer Aortenruptur
- Plötzlicher, extremer Vernichtungsschmerz
- Abdominale Aortenruptur
: Starke abdominelle oder lumbale Schmerzen - Thorakale Aortenruptur
: Retrosternale oder interskapuläre Schmerzen
- Abdominale Aortenruptur
- Akuter Volumenmangelschock
(Hypotonie, Tachykardie , Blässe, Kaltschweißigkeit) - Bewusstseinsverlust/Synkope
- Retroperitoneale Blutung:
- Grey-Turner-Zeichen
(Flankenhämatome) - Cullen-Zeichen
(periumbilikale Hämatome )
- Grey-Turner-Zeichen
- Freie intraabdominelle Blutung → Rasche hämodynamische Instabilität, Kreislaufstillstand
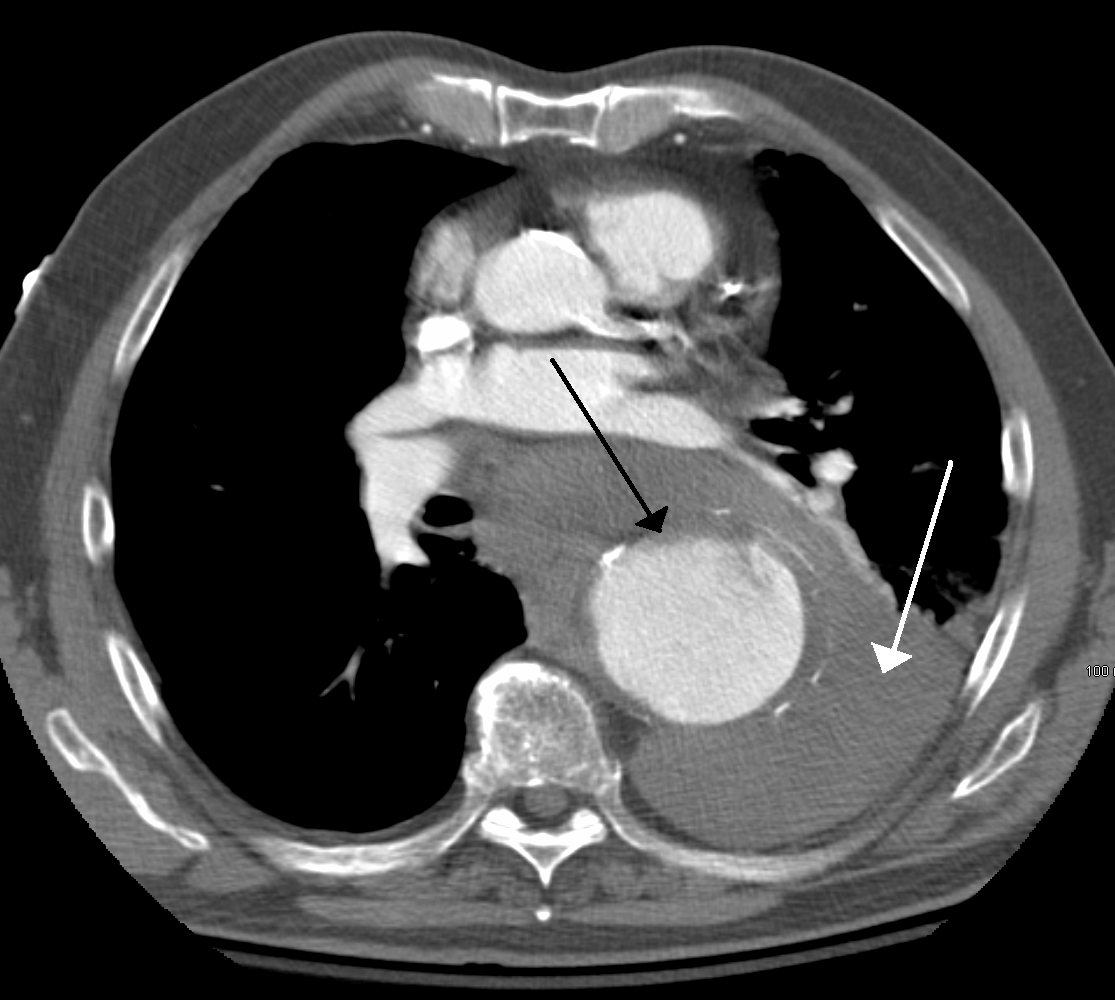
CTRupturedTA, https://commons.wikimedia.org/wiki/File:CTRupturedTA.PNG, James Heilman, MD, CC BY-SA 3.0, https://creativecommons.org/licenses/by-sa/3.0, via Wikimedia Commons
InfoEine drohende Aneurysmaruptur
kann sich radiologisch durch einen schnell zunehmenden Aortendurchmesser und durch periaortale Flüssigkeit zeigen.
Spezifische Komplikationen
Aortendissektion Stanford Typ A:
- Myokardinfarkt bei Verlegung der Koronararterien
- Aortenklappeninsuffizienz
- Bei Dissektion der Aortenwurzel → unzureichender Klappenschluss
- Perikardtamponade
bis hin zum obstruktiven Schock - Ischämischer Schlaganfall
bei Verlegung der hirnversorgenden Arterien
Aortendissektion Stanford Typ A und Stanford Typ B:
- Pleuraerguss
- Synkope
- Blutungen
- Gefäßverlegungen
- Truncus coeliacus
, Mesenterialarterien → Akutes Abdomen durch Darmischämie - Nierenarterien → Akutes Nierenversagen
mit Oligurie /Anurie - Extremitätenarterien → Akute Beinischämie mit blassen, pulslosen Beinen
- A. spinalis anterior → Querschnittssyndrom
- Symptome: Paraparese, Hypästhesie, Blasen
-/Darmstörung
- Symptome: Paraparese, Hypästhesie, Blasen
- Verlegung der gesamten distalen Aorta
: Leriche Syndrom (Minderperfusion der Beine; bei chronischer Form auch Potenzstörungen, Schmerzen in Gesäß, Hüfte und Oberschenkeln und Blasenentleerungsstörungen)
- Truncus coeliacus
Chronische Komplikationen:
- Aneurysmatische Erweiterung und Spätruptur
- Persistierende Dissektion kann zur progressiven Dilatation der Aorta
führen - Hohes Risiko für spätere Ruptur → regelmäßige Verlaufskontrolle nötig
- Persistierende Dissektion kann zur progressiven Dilatation der Aorta
- Rezidivdissektion oder Progression
- Fortgesetzte Dissektion trotz Therapie möglich
- Besonders bei unzureichender Blutdruckkontrolle
- Chronische Malperfusion
- Langfristige Organminderperfusion durch Gefäßkompression
- Symptome: Chronische Niereninsuffizienz
, Angina pectoris , Claudicatio intermittens
Für die Komplikationen nach chirurgischer und interventioneller Therapie siehe auch Abschnitt Komplikationen und Nachsorge im Artikel Aortenaneurysma
Prävention/Nachsorge
Für die Nachsorge nach chirurgischer und interventioneller Therapie (z.B. Nachsorge nach einer (T)EVAR
- Blutdruckkontrollen und konsequente Blutdruckeinstellung auf unter 130/80 mmHg, vorzugsweise mit ß-Blockern
- Ggf. Lipidmanagement mit Statinen
- Lebensstilveränderung
im Sinne der kardiovaskulären Prävention
Prognose
Die Prognose einer Aortendissektion hängt entscheidend von der Lokalisation, dem Zeitpunkt der Diagnosestellung, der raschen Therapieeinleitung sowie dem Vorliegen von Komplikationen ab.
- Eine Aortendissektion Stanford Typ A hat eine Mortalität von ca. 1-2% pro Stunde nach Symptombeginn
- Ohne chirurgische Behandlung beträgt die Mortalität bei einer akuten Aortendissektion ca. 24% innerhalb der ersten 24 Stunden, ca. 29% nach 48 Stunden und ca. 44% nach 7 Tagen
- Bei chirurgischer Therapie beträgt die Mortalität ca. 10% innerhalb der ersten 24 Stunden, ca. 12% innerhalb der ersten 48 Stunden und ca. 16% innerhalb der ersten 7 Tage
- Eine unkomplizierte Aortendissektion Typ B weist eine 30-Tage-Mortalität von 10% auf
- Bei einer Operation aufgrund einer ischämischen Komplikation besteht eine Mortalität von 25% innerhalb der ersten 30 Tage
- 10-Jahres-Überlebensrate von Patient:innen, die Krankenhaus verließen nach Aortendissektion: 30-60%
Risikofaktoren für schlechte Prognose:
- Malperfusion von Organen
- Schock
- Höheres Alter
Quellen
- S2k-Leitlinie Behandlung der Thorakalen Aortendissektion Typ A, Deutsche Gesellschaft für Thorax-, Herz- und Gefäßchirurgie e.V. (DGTHG)
- S2k-Leitlinie Typ B Aortendissektion, Deutsche Gesellschaft für Thorax-, Herz- und Gefäßchirurgie e.V. (DGTHG)
- Acute Aortic Syndromes, Thomas T. Tsai, MD, Christoph A. Nienaber, MD, and Kim A. Eagle, MD, Circulation, Volume 112, Number 24, https://doi.org/10.1161/CIRCULATIONAHA.105.534198



