Zusammenfassung
Die Multiple Sklerose (MS) ist eine autoimmun vermittelte, chronisch-entzündliche Erkrankung des zentralen Nervensystems, die durch multifokale, demyelinisierende Läsionen mit sekundärer axonaler Schädigung gekennzeichnet ist.
DefinitionDie Multiple Sklerose ist eine autoimmun vermittelte, chronisch-entzündliche ZNS-Erkrankung mit multifokalen, herdförmigen Entmarkungen sowie axonaler Schädigung.
Die Prävalenz weist eine deutliche Abhängigkeit vom Breitengrad auf. In mitteleuropäischen Ländern stellt MS die häufigste chronisch-entzündliche ZNS-Erkrankung dar. Frauen sind insgesamt deutlich häufiger betroffen.
Die genaue Ursache der Erkrankung ist nicht geklärt. Die Ätiologie gilt als multifaktoriell und beruht auf einem komplexen Zusammenspiel genetischer Dispositionen und Umweltfaktoren.
Pathophysiologisch stehen fehlgeleitete Immunreaktionen im Vordergrund, die zu regionalen Entzündungsprozessen, Demyelinisierung und im Verlauf auch zu Schädigungen von Axonen und Neuronen führen.
Das klinische Bild ist sehr variabel, da die entzündlich-demyelinisierenden Läsionen in verschiedenen Bereichen des ZNS auftreten können. Zu den häufigsten Erstsymptomen zählen Optikusneuritis, Sensibilitätsstörungen sowie Fatigue. Die Erkrankung verläuft meist schubförmig.
Für die Diagnosestellung sind neben der Anamnese und der klinisch-neurologischen Untersuchung vor allem MRT- und Liquorbefunde wegweisend. Als Ausschlussdiagnose setzt sie voraus, dass alternative Ursachen der Symptome hinreichend ausgeschlossen wurden.
Das therapeutische Konzept der MS gliedert sich in drei zentrale Säulen:
- Schubtherapie: meist hochdosierte Glucocorticoide
- Verlaufsmodifizierende Therapie: langfristige immunmodulatorische Stufentherapie
- Symptomatische Therapie: medikamentöse und nicht-medikamentöse Maßnahmen
MerkeObwohl keine kurative Therapie existiert, hat sich die Langzeitprognose durch moderne immunmodulatorische Strategien deutlich verbessert.
Epidemiologie
- Geografische Verteilung:
- Weltweit etwa 2,8 Millionen Erkrankte
- Prävalenz abhängig vom Breitengrad ("Nord-Süd-Gradient"):
- Höhere Prävalenz in nördlichen und südlichen Breiten (z.B. Kanada, Nordamerika, Europa)
- Niedrigere Prävalenz in Äquatornähe (z.B. Südostasien, Afrika)
- Prävalenz in Deutschland: ca. 250–300 pro 100.000 Einwohner:innen
- Manifestationsalter: typischerweise zwischen dem 20. und 40. Lebensjahr (Häufigkeitsgipfel um 30. Lebensjahr)
- Geschlechtsverteilung:
- Frauen sind etwa 2-3 Mal so häufig betroffen wie Männer
- Ausnahme: primär progrediente MS (PPMS) → Verhältnis etwa 1:1
MerkeIn Mitteleuropa ist die MS die häufigste chronisch-entzündliche Erkrankung des zentralen Nervensystems.
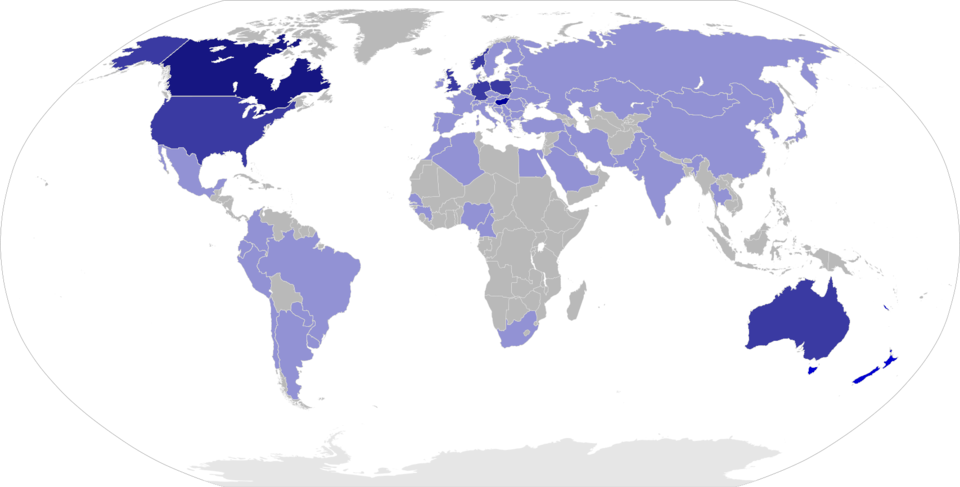
“Multiple Sclerosis Prevalence.png” von Adert https://commons.wikimedia.org/wiki/File:Multiple_Sclerosis_Prevalence.png, CC BY-SA 3.0 https://creativecommons.org/licenses/by-sa/3.0 via Wikimedia Commons
Ätiologie
Die genaue Ursache der Multiplen Sklerose ist bis heute nicht geklärt. Es handelt sich um eine Autoimmunerkrankung des zentralen Nervensystems, bei der das Immunsystem körpereigene Myelinstrukturen angreift. Ein spezifischer Autoantikörper konnte bislang jedoch nicht identifiziert werden.
Die Ätiologie gilt als multifaktoriell und basiert auf einem komplexen Zusammenspiel unterschiedlicher Faktoren:
Genetische Prädisposition:
- Familiäre Häufung als Hinweis auf genetische Komponente:
- Risiko für Verwandte 1. Grades etwa 10- bis 20-fach erhöht (Erkrankungsrisiko etwa 2-4 %, gegenüber 0,1-0,2 % in der Normalbevölkerung)
- Konkordanzrate bei eineiigen Zwillingen: 25–30 %
- Genetische Risikofaktoren:
- Stärkster genetischer Risikofaktor: HLA-DR15
- Beispiele weiterer Risikogene: L2RA, IL7R, TNFRSF1A
Umweltfaktoren:
- Vitamin-D
-Mangel: - Zusammenhang mit Breitengrad: höhere Prävalenz in Regionen mit geringer Sonneneinstrahlung
- Hinweise auf protektive Effekte einer ausreichenden Vitamin-D
-Versorgung
- Rauchen: regelmäßiges Rauchen erhöht das Erkrankungsrisiko um ca. 50 %
- Mikrobiom
- Übergewicht
: insbesondere Adipositas in der frühen Adoleszenz - Bakterielle und virale Infektionen:
- Epstein-Barr-Virus (EBV): gilt als bedeutendster infektiöser Risikofaktor
- Weitere Infektionserreger: Humanes Herpesvirus 6, Chlamydien
, Rickettsien , Masern
InfoNach aktuellem Kenntnisstand wird eine Infektion mit dem Epstein-Barr-Virus als notwendige, jedoch nicht alleinige Bedingung für die Entstehung der MS angesehen. Da die meisten EBV-infizierten Personen keine MS entwickeln, müssen weitere prädisponierende Faktoren an der Pathogenese beteiligt sein.
Pathophysiologie
Grunprinzipien
Die Pathophysiologie der Multiplen Sklerose ist komplex und bis heute nicht vollständig verstanden. Gesichert ist, dass fehlgeleitete Immunprozesse eine chronisch-entzündliche Schädigung von Myelin und Axonen im ZNS verursachen. Die genauen auslösenden Mechanismen und Wechselwirkungen zwischen Immun- und Nervensystem bleiben jedoch in vielen Aspekten weiterhin nicht abschließend geklärt.
Autoimmunreaktion
Periphere Aktivierung von T-Lymphozyten:
- Versagen peripherer und zentraler Immuntoleranzmechanismen → Aktivierung autoreaktiver T-Zellen in der Peripherie
- Aktivierte T-Zellen exprimieren Adhäsionsmoleküle und proinflammatorische Zytokine → Permeabilität der Blut-Hirn-Schranke↑
- T-Zellen, B-Zellen, Monozyten und andere Immunzellen können die Blut-Hirn-Schranke passieren und ins ZNS eindringen
Klonale Expansion & Reaktivierung:
- Eingewanderte T-Zellen treffen auf ZNS-ansässige antigenpräsentierende Zellen (insb. Mikroglia, perivaskuläre Makrophagen
und Astrozyten) - Antigenpräsentierende Zellen präsentieren myelinspezifische Antigene → klonale Expansion und Reaktivierung der T-Zellen
Fehlgeleitete Immunantwort:
- Nach erneuter Aktivierung identifizieren die T-Zellen verschiedene Myelinbestandteile fälschlicherweise als Antigene (z.B. basisches Myelinprotein oder Myelin-Oligodendrozyten-Glykoprotein)
- Die Bindung führt zur Freisetzung proinflammatorischer Mediatoren und damit zur direkten Schädigung von Oligodendrozyten und Myelinscheiden
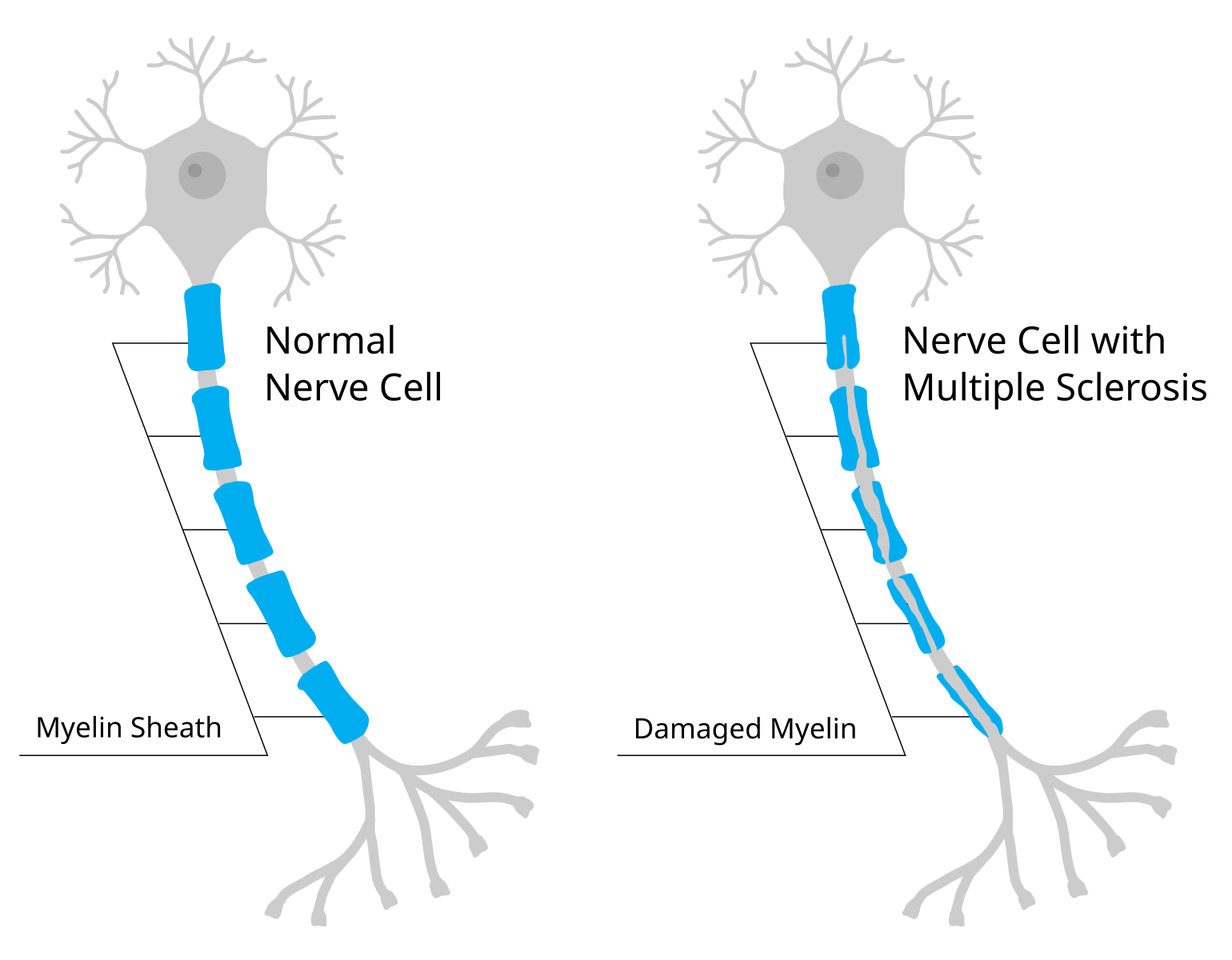
“Myelin sheath damage in multiple sclerosis.svg” von Mjeltsch https://commons.wikimedia.org/wiki/File:Myelin_sheath_damage_in_multiple_sclerosis.svg CC BY-SA 4.0 https://creativecommons.org/licenses/by-sa/4.0 via Wikimedia Commons
Verstärkung der Entzündungsreaktion:
- Die Freisetzung proinflammatorischer Zytokine und Chemokine führt zur…
- Aktivierung von Mikrogliazellen und Astrozyten
- Rekrutierung und Aktivierung von Makrophagen
und B-Zellen
(das Zusammenwirken von T- & B-Zellen führt zu einer entzündlichen
Markscheidenschädigung, die als typisches Charakteristikum der MS gilt) - Stimulation der Antikörperproduktion in Plasmazellen
- Aktivierung des Komplementsystems
Klinik
Die Multiple Sklerose ist durch individuell unterschiedliche Krankheitsverläufe und eine ausgeprägte Heterogenität der Symptomatik gekennzeichnet, da die entzündlich-demyelinisierenden Läsionen in verschiedenen Bereichen des ZNS auftreten können. Die jeweils vorherrschenden neurologischen Symptome reflektieren dabei unmittelbar die topographische Verteilung der aktiven Entmarkungsherde.
Häufige MS-Symptome
MerkeZu den häufigsten Erstsymptomen der Multiplen Sklerose zählen Optikusneuritis, Sensibilitätsstörungen sowie chronische Erschöpfung (Fatigue).
Okuläre Störungen:
- Optikusneuritis (Neuritis nervi optici):
- Entzündung des Sehnervs mit Demyelinisierung → betrifft i.d.R. den retrobulbären Anteil des N. opticus (Retrobulbärneuritis):
- Akute, meist einseitige Visusminderung
- Bulbusbewegungsschmerz
- Sehr häufig: zentrale Gesichtsfelddefekte (Zentralskotom)
- Photophobie
- Farbsinnstörung (Farbentsättigung)
- Entzündung des Sehnervs mit Demyelinisierung → betrifft i.d.R. den retrobulbären Anteil des N. opticus (Retrobulbärneuritis):
- Störungen der Okulomotorik:
- Doppelbilder durch Augenmuskelparesen (meist Abduzensparese)
- Internukleäre Ophtalmoplegie (INO): Läsion des Fasciculus longitudinalis medialis im Hirnstamm
→ Adduktionsdefizit des ipsilateralen Auges
TippRetrobulbärneuritis - Klinischer Spruch: „Der Patient sieht nichts und der Arzt sieht auch nichts." (→ initial häufig unauffälliger Ophthalmoskopiebefund)
Motorische Störungen:
- Zentrale Paresen (v.a. spastische Lähmungen):
- Gesteigerte Muskeleigenreflexe
und abgeschwächte Fremdreflexe (z.B. Bauchhautreflex ↓) - Spastische Tonuserhöhung
- Positive Pyramidenbahnzeichen
- Gesteigerte Muskeleigenreflexe
Sensibilitätsstörungen:
- Parästhesien (insb. Kribbeln und Brennen), Hypästhesien, Dysästhesien:
- Oft segmental oder einseitig betont
- Häufig betroffen: obere und untere Extremitäten (insb. Füße und Unterschenkel)
InfoLhermitte-Zeichen
- Definition: das Lhermitte-Zeichen (positives Nackenbeugezeichen) ist ein prüfbares klinisches Phänomen im Rahmen der neurologischen Untersuchung und entsteht typischerweise durch Irritationen der dorsalen Hinterstränge im Bereich des Zervikalmarks.
- Überprüfung: zur Prüfung wird der Kopf der Patient:innen passiv in die Flexion bewegt. Ein positives Lhermitte-Zeichen äußert sich durch plötzlich auftretende, elektrisierende Parästhesien entlang der Wirbelsäule (von kranial nach kaudal absteigend).
Infratentorielle Störungen:
- Nystagmus
- Dysphagie
- Schwindel
- Ataxie
(Koordinationsstörungen): - Gangataxie, Standataxie
- Dysmetrie der Extremitäten
- Intentionstremor
- Dysdiadochokinese
- Ataktische Dysarthrie
mit “skandierendem” Sprechen: abgehackte, unregelmäßige Sprache)
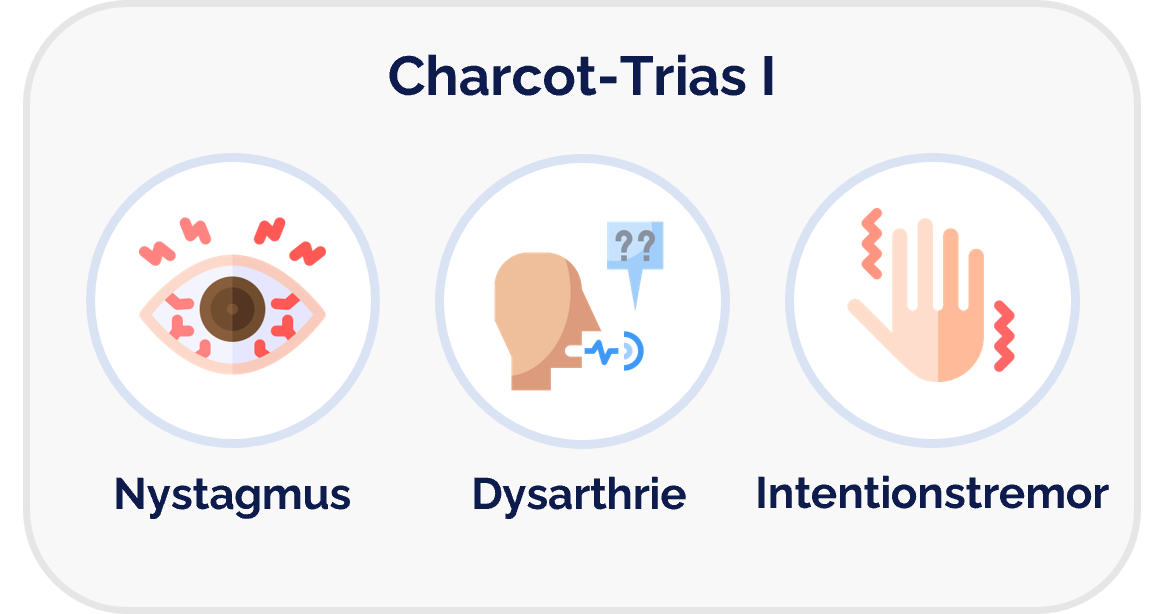
DefinitionCharcot-Trias I
Die Charcot-Trias I bezeichnet ein kombiniertes Auftreten von Intentionstremor
, Nystagmus und skandierender Sprache (Dysarthrie ). Dieser Symptomkomplex weist typischerweise auf eine Schädigung im Bereich des Cerebellums hin, wie sie unter anderem bei Multipler Sklerose auftreten kann.
Autonome Störungen:
- Blasenstörungen (Harndrang, Inkontinenz
, Harnverhalt ) - Darmstörungen (Obstipation
, selten Stuhlinkontinenz) - Sexuelle Funktionsstörungen:
- ♂: Ejakulationsstörung, erektile Dysfunktion, Libidoverlust
- ♀: Lubrikationsstörung, Libidoverlust
Weitere Symptome:
- Fatigue (sehr häufig!)
- Schmerzen:
- Kopfschmerzen
- Neuropathische Schmerzen
- Muskuloskelettale Schmerzen (z.B. als Folge der Spastik
)
- Kopfschmerzen
- Kognitive und psychische Störungen:
- Gehäuftes Auftreten von depressiven Episoden und Angststörungen
- Konzentrations- und Gedächtnisstörungen
DefinitionDas Uhthoff-Phänomen beschreibt eine vorübergehende Verschlechterung neurologischer Symptome bei Patient:innen mit demyelinisierenden Erkrankungen infolge einer Erhöhung der Körpertemperatur
. Zu den typischen Auslösern zählen unter anderem körperliche Anstrengung, Fieber oder eine warme Umgebung.
Verlaufsformen
Klinische Verlaufsformen
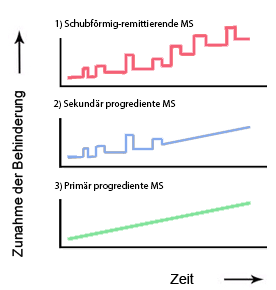
“Typen der MS.png” von Garak76 https://commons.wikimedia.org/wiki/File:Typen_der_MS.png, CC BY-SA 3.0 http://creativecommons.org/licenses/by-sa/3.0/ via Wikimedia Commons
Das Bild wurde zugeschnitten, die Farbe der Graphen verändert und Beschriftungen hinzugefügt.
- Schubförmig-remittierende MS (RRMS):
- Häufigste Form: ca. 85 % der Fälle bei Erstdiagnose
- Charakteristika:
- Akut auftretende neurologische Defizite (schubweise)
- Teilweise oder vollständige Rückbildung der Symptome zwischen den Schüben
- Zwischen den Schüben keine Behinderungszunahme
- Sekundär progrediente MS (SPMS):
- Häufigkeit: in ca. 50 % der Fälle geht die RRMS in eine SPMS über
- Charakteristika:
- Entwickelt sich nach vorherigem schubförmigem Verlauf
- Gekennzeichnet durch kontinuierliche Zunahme der Behinderung
- Häufig weiterhin gelegentliche Schübe
- Primär progrediente MS (PPMS):
- Häufigkeit: ca. 10-15 % der Erstmanifestationen
- Charakteristika:
- Von Beginn an progrediente Behinderungszunahme
- Kein vorheriger schubförmiger Verlauf
MerkeDie Erkrankung verläuft meist schubförmig und beginnt in der Regel monosymptomatisch. Es sind jedoch auch langsame, kontinuierlich fortschreitende Verlaufsformen möglich.
Sonderformen
- Radiologisch isoliertes Syndrom (RIS):
- Nachweis typischer MS-Läsionen im MRT, ohne anamnestische oder klinische Symptomatik (häufig Zufallsbefund)
- Etwa 50 % der Betroffenen entwickeln innerhalb von 10 Jahren klinische Symptome einer MS
- Klinisch isoliertes Syndrom (KIS/CIS):
- Entzündlich-demyelinisierendes Ereignis im ZNS (z.B. Optikusneuritis), das mind. 24 Stunden anhält und typisch für MS ist, die Diagnosekriterien jedoch nicht vollständig erfüllt.
- Erste klinische Manifestation einer möglichen MS
Diagnostik
Die Diagnostik der Multiplen Sklerose dient dem Nachweis einer immunvermittelten, entzündlich-demyelinisierenden Erkrankung des zentralen Nervensystems, die durch zeitlich und räumlich disseminierte Läsionen gekennzeichnet ist.
Multiple Sklerose ist zudem eine Ausschlussdiagnose und darf nur gestellt werden, wenn andere mögliche Ursachen für die vorliegenden klinischen Beschwerden ausgeschlossen wurden.
Klinische Untersuchung
Anamnese:
- Aktuelle Symptomatik und zeitliche Dynamik der Beschwerden: Art der Symptome, Beginn, Dauer, Verlauf?
- Typische Erst- und Folgeereignisse: z.B. Optikusneuritis (Sehverschlechterung, Schmerzen bei Augenbewegung)
- Hinweise auf zurückliegende Schübe (z.B. Episoden mit Sensibilitäts- oder Sehstörungen)
- Vorgeschichte: z.B. Infektgeschichte, andere systemische Erkrankungen etc.
- Familienanamnese: chronisch-entzündliche ZNS- oder Autoimmunerkrankung in der Familie?
Neurologische Untersuchung
Die neurologische Untersuchung
AchtungBei Verdacht auf eine chronisch-entzündliche Erkrankung des zentralen Nervensystems ist eine umfassende neurologische Untersuchung
unerlässlich, um die beschriebenen neurologischen Defizite objektiv zu überprüfen.
MerkeAufgrund der heterogenen topografischen Verteilung der ZNS-Läsionen (örtliche Dissemination) kann die Multiple Sklerose ein sehr variables klinisches Erscheinungsbild haben.
Apparative Diagnostik - MRT
- Verfahren: kranielle und spinale MRT (primäre Bildgebung zur Diagnostik und Verlaufsbeobachtung bei MS)
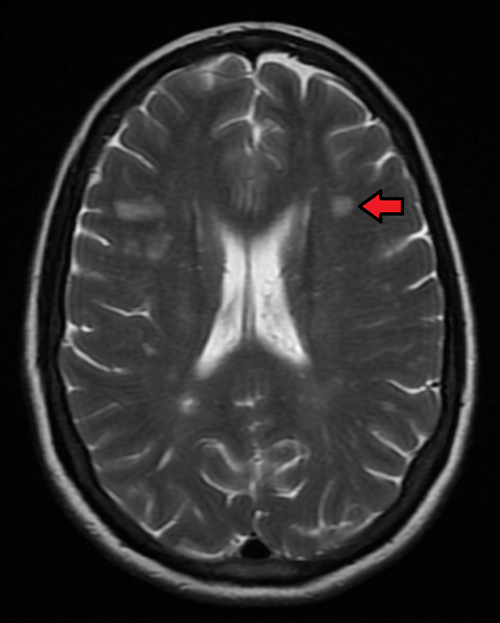
“MSMRIMark.png” von James Heilman https://commons.wikimedia.org/wiki/File:MSMRIMark.png, CC BY-SA 4.o https://creativecommons.org/licenses/by-sa/4.0 via Wikimedia Commons
- Befund: multilokuläre Läsionen
- Typische Lokalisationen:
- Periventrikuläres Marklager, insb. im Balken
- Juxtakortikal/kortikal (hilfreich zur Differenzierung von vaskulären Läsionen)
- Infratentoriell, insb. im Pons
- Intraspinal: meist zervikal, gelegentlich thorakal; typischerweise monosegmental
- Morphologie:
- Meist oval oder länglich, gelegentlich rundlich
- Periventrikuläre Läsionen: häufig länglich und radial verlaufend („Dawson´s Fingers“)
- Signalverhalten:
- T2-gewichtete und FLAIR-Sequenzen: hyperintense Läsionen
- T1-gewichtete Sequenzen:
- Akute Läsionen: meist iso- bis leicht hypointens
- Chronische Läsionen: deutlich hypointens → sogenannte „Black Holes“ → Hinweis auf irreversiblen axonalen Verlust (prognostisch ungünstige Gewebedestruktion)
- MRT mit Kontrastmittel (Gadolinium): dient vor allem der Darstellung akuter, aktiver Krankheitsherde → akute Läsionen zeigen sich hyperintens (Aufnahme von Gadolinium als Ausdruck der Schrankenstörung)
- Typische Lokalisationen:
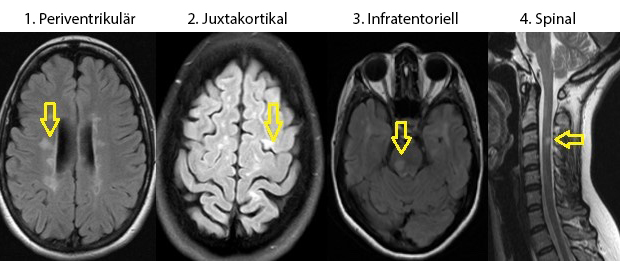
“Diseminacion en espacio.jpg” von DraazucenaDL https://commons.wikimedia.org/wiki/File:Diseminacion_en_espacio.jpg, CC BY-SA 4.0 https://creativecommons.org/licenses/by-sa/4.0 via Wikimedia Commons. Die Beschriftungen wurden übersetzt und entsprechend ausgetauscht.
Liquordiagnostik
- Diagnostischer Stellenwert:
- Unterstützung der Diagnose: ein positiver Befund kann in bestimmten Fällen als optionales Diagnosekriterium (siehe Diagnosekriterien) dienen, falls die MRT-Kriterien nicht vollständig erfüllt sind
- Wesentlich für Differentialdiagnostik
- Wichtige Parameter:
- Zellzahl und Differenzialzellbild:
- Zellzahl: i.d.R. normal bis leicht erhöht
- Differenzialzellbild: lymphomonozytäre Pleozytose, häufig kleiner Anteil aktivierter Plasmazellen
- Gesamteiweiß: meist normal bis leicht erhöht (unspezifischer Marker für Proteinveränderungen im Liquorraum)
- Albumin
-Liquor-Serum -Quotient: meist normal bis leicht erhöht (deutlicher Anstieg spricht für eine ausgeprägte Schrankenstörung → Hinweis auf andere Diagnose) - Glucose
& Laktat: i.d.R. normwertig - Oligoklonale Banden (OKB):
- Positivität: ≥2 CSF-spezifische Banden („Typ 2“ oder „Typ 3“ Muster)
- Sensitivität
: 85–95 % bei MS
- Kappa-freie Leichtketten (kFLC)
- Intrathekale Immunglobulinsynthese im Reiber-Diagram: IgG-Index bei ca. 70 % der Patient:innen erhöht
- MRZ-Reaktion:
- MRZ = Masern
-, Röteln -, Varizella-Zoster-Antikörper-Indizes - Positiv, wenn mind. zwei der drei Indizes erhöht sind
- Hochspezifisch (ca. 98 %) für MS, jedoch nur bei etwa 60 % der Patient:innen positiv
- MRZ = Masern
- Bei positivem Serum
-Befund: Borrelien - & Lues-Serologie im Liquor
- Zellzahl und Differenzialzellbild:
Blut- und Urindiagnostik
Die Blut- und Urindiagnostik
Laut aktueller DGN-Leitlinie werden diese Untersuchungen - abgesehen von Borrelien
MerkeIm Rahmen der Abklärung von Multipler Sklerose sollen nach aktuellem Stand der Forschung MRT-Aufnahmen mit standardisierten Sequenzen sowie eine Liquoruntersuchung erfolgen. Weiterführende Laboruntersuchungen zur breiten Differentialdiagnostik sind nur bei konkretem klinischem Verdacht notwendig.
Elektrophysiologische Diagnostik
Elektrophysiologische Untersuchungen dienen dazu, die Funktionsfähigkeit zentraler Nervenbahnen objektiv zu prüfen und demyelinisationsbedingte Leitungsverzögerungen nachzuweisen.
- Befund: Verzögerung der Latenzzeiten als Hinweis auf gestörte Erregungsleitung
- Häufige Verfahren:
- Visuell evozierte Potenziale (VEP): pathologische Verzögerung bei ca. 80 % der Patient:innen
- Somatosensorisch evozierte Potenziale (SEP)
- Motorisch evozierte Potenziale (MEP): verzögerte MEP bei Schädigung der Pyramidenbahn
- Akustisch evozierte Potenziale (AEP)
Diagnosekriterien
McDonald-Kriterien
Für die Diagnosestellung der Multiplen Sklerose haben sich die sogenannten McDonald-Kriterien etabliert, welche im Wesentlichen klinische Krankheitsschübe im Zusammenhang mit MRT-Befunden bewerten. Dabei wird vorausgesetzt, dass andere mögliche Ursachen für die vorliegenden klinischen Beschwerden ausgeschlossen werden können.
MerkeDie Diagnose der Multiplen Sklerose setzt voraus, dass andere Ursachen bzw. potenzielle Differentialdiagnosen für die klinische Präsentation ausgeschlossen werden können.
Räumliche und zeitliche Dissemination:
Die Diagnosekriterien basieren primär auf dem Nachweis einer räumlichen und zeitlichen Dissemination des entzündlich-demyelinisierenden Geschehens im ZNS. Damit ist gemeint, dass Entzündungs- bzw. Demyelinisationsherde an unterschiedlichen Lokalisationen des ZNS (dissemination in space, DIS) und zu verschiedenen Zeitpunkten (dissemination in time, DIT) nachzuweisen sind.
InfoDer Nachweis einer räumlichen Dissemination im MRT ist – abgesehen von einer definierten Ausnahme – für die Diagnosestellung obligatorisch. Gemäß den aktuellen McDonald-Kriterien wird die zeitliche Dissemination hingegen nicht mehr zwingend vorausgesetzt, sofern die übrigen diagnostischen Kriterien erfüllt sind.
Kriterien für die Diagnose der schubförmigen MS:
| Anzahl der Schübe | Objektive Läsionen | Zusätzlich erforderliche Kriterien |
| 2 oder mehr | 2 oder mehr | Keine |
| 2 oder mehr | 1 |
|
| 1 | 2 oder mehr |
|
| 1 | 1 | Räumliche und zeitliche Dissemination |
Kriterien für die Diagnose der primär progredienten MS:
- Klinische Progression über mind. 12 Monate (prospektiv oder retrospektiv) PLUS zwei der folgenden Kriterien:
- Eine oder mehrere T2-hyperintense Läsion in mind. einem der folgenden Areale: periventrikulär, kortikal/juxtakortikal, infratentoriell, N. opticus
- Mind. zwei T2-hyperintense Läsionen spinal
- Nachweis von liquorspezifischen oligoklonalen Banden (OKB) oder intrathekal produzierten freien Kappa-Leichtketten
AchtungEntsprechend der McDonald-Kriterien 2024 ist eine rein klinische Diagnosestellung nicht mehr zulässig. Voraussetzung für die Diagnose sind typische Läsionen im MRT.
Klinische Scoring-Instrumente
Expanded Disability Status Scale
Die Expanded Disability Status Scale (EDSS) ist ein Instrument zur quantitativen Erfassung des Behinderungsgrades bei Patient:innen mit Multipler Sklerose. Sie ermöglicht eine strukturierte Bewertung verschiedener neurologischer Funktionssysteme sowie der Gehfähigkeit und somit eine standardisierte Verlaufs- und Therapieevaluation.
Die Skala umfasst Werte von 0 bis 10 und bildet damit den Verlauf von vollständiger neurologischer Integrität (0) bis hin zu schwerster Behinderung bzw. dem Tod infolge der MS (10) ab. Die Gradeinteilung basiert auf der Untersuchung folgender funktioneller Systeme:
- Pyramidenbahn
(Motorik) - Kleinhirn (Koordination, Gleichgewicht)
- Hirnstamm
(Augenmotorik, Schlucken, Artikulation ) - Sensorik
- Blasen
- und Darmfunktion - Sehfunktion
- Zerebrale Funktionen (Kognition, Stimmung)
- Sonstige Funktionen
Pathologie
Morphologische Veränderungen:
- MS-Läsion (Plaque
): - Herdförmige inflammatorische Schädigungen im ZNS
- Abbau der Myelinscheiden (Demyelinisierung) und sekundäre axonale Degeneration
- In späteren Stadien auch Neuronenverlust
Lokalisation & Verteilung:
- Vorwiegend betroffen: weiße Substanz (im Verlauf zunehmende Beteiligung der grauen Substanz)
- Typische Prädilektionsstellen:
- Periventrikuläres und juxtakortikales Marklager („Dawson’s Fingers“)
- Hirnstamm
(insb. Pons) - Kleinhirn und Kleinhirnstiele
- Pyramidenbahn
- Sehnerven
- Rückenmark (insb. Hinterstränge)
- Klinische Relevanz: Symptome abhängig von Läsionslokalisation (z.B. Optikusneuritis, Paresen)
Histologische Klassifikation:
Die multifokalen Entmarkungszonen zeigen je nach Aktivitätsstadium charakteristische histologische Veränderungen:
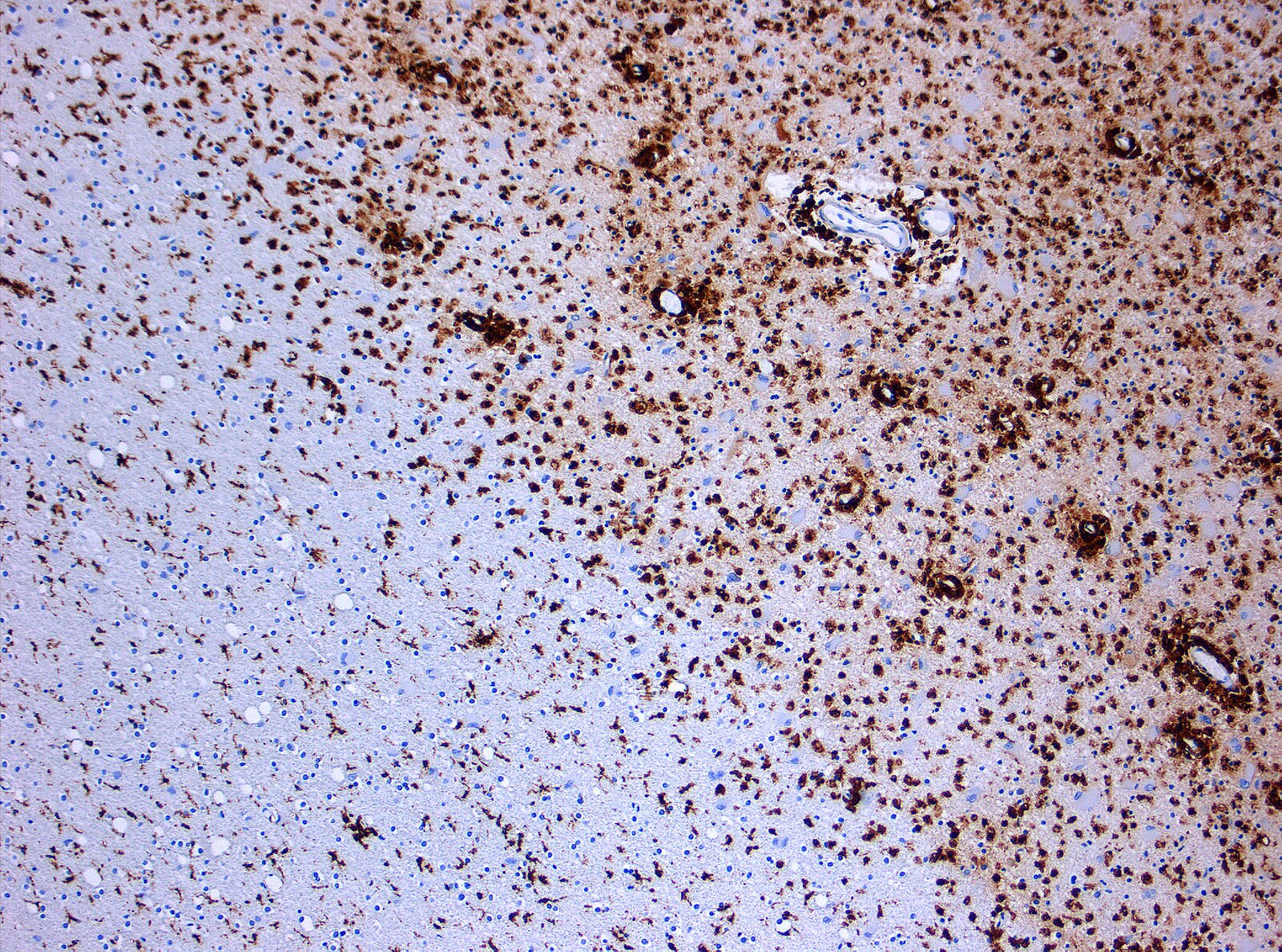
“MS Demyelinisation CD68 10x.jpg” von Marvin 101 https://commons.wikimedia.org/wiki/File:MS_Demyelinisation_CD68_10x.jpg, CC BY-SA 3.0 http://creativecommons.org/licenses/by-sa/3.0/ via Wikimedia Commons.
- Aktive Plaques:
- Deutliche Entzündungsaktivität
- Dichtes lymphozytäres Infiltrat
- Makrophagen
mit aufgenommenen Myelinabbauprodukten - Ausgeprägter Markscheidenabbau (Demyelinisierung)
- Inaktive Plaques:
- Vollständige Demyelinisierung
- Ausgeprägte astrozytäre Vernarbung
(Gliosis) - Verminderte Axondichte
Neuropathologische Kernmerkmale:
- Inflammation
- Demyelinisierung
- Remyelinisierung (Schattenplaques)
- Neurodegeneration
- Gliöse Vernarbung
Veränderungen im weiteren Verlauf:
- Übergang von fokaler zu diffuser Entzündungsaktivität
- Kortikale und subkortikale Atrophie
- Verlust von Synapsen und Neuronen → klinisch progrediente Behinderung
Differentialdiagnosen
Andere entzündlich-demyelinisierende Erkrankungen:
- Akute disseminierte Enzephalomyelitis (ADEM)
- Neuromyelitis optica (NMO)/Neuromyelitis-optica-Spektrum-Erkrankung (NMOSD)
- MOG-Antikörper-assoziierte Erkrankung (MOGAD)
Infektionskrankheiten:
- Chronische Neuroborreliose
- Neurosyphilis
- Progressive multifokale Leukenzephalopathie (JC-Virus)
- HIV-Infektion
AchtungInfektiöse Differentialdiagnosen müssen bei atypischem Verlauf, hoher Zellzahl oder systemischen Symptomen immer ausgeschlossen werden!
Metabolische/hereditäre Erkrankungen:
- Vitamin-B12
-Mangel (Funikuläre Myelose) - Kupfermangel
- Leukodystrophien (z.B. Adrenoleukodystrophie)
- Mitochondriopathien
Systemische Autoimmunerkrankungen:
- Neurosarkoidose
- Sjögren-Syndrom
- Systemischer Lupus erythematodes
Therapie
Das therapeutische Konzept der Multiplen Sklerose gliedert sich in drei zentrale Säulen:
- Schubtherapie
- Verlaufsmodifizierende Therapie (Immuntherapie)
- Symptomatische Therapie
Schubtherapie
Schubtherapie
Das primäre Ziel der Schubtherapie besteht in einer möglichst schnellen Remission der klinischen Symptomatik. Diese wird insbesondere durch die antiinflammatorische Wirkung der Glucocorticoide
DefinitionAls Schub bezeichnet man neu auftretende oder deutlich progrediente neurologische Symptome, die mind. 24 Stunden anhalten, nach einer klinisch stabilen Phase von mind. 30 Tagen auftreten und nicht durch Fieber, Infektionen oder andere Ursachen erklärt werden können.
Glucocorticoid
- Gabe hochdosierter Glucocorticoide
als Therapie der Wahl: - Methylprednisolon 500-1000 mg/Tag i.v. über 3–5 Tage
- Anschließend ggf. orale Ausschleichphase über 1–2 Wochen
- Bei unzureichender Besserung der Schubsymptomatik: Eskalationstherapie mit höherer Glucocorticoid
-Dosis oder verlängerte Therapie für bis zu 10 Tage
- Allgemeine Hinweise zur Glucocorticoidtherapie bei MS:
- Vor Therapiebeginn sollten folgende Untersuchungen durchgeführt werden:
- Ausschluss eines Infekts (Urinkultur
, Routinelabor) - Bestimmung von Blutzucker und Elektrolyten
- Bei Frauen in gebärfähigem Alter und unklarem Status: Schwangerschaftstest
- Ausschluss eines Infekts (Urinkultur
- Therapiebegleitende Maßnahmen:
- Regelmäßige Kontrolle von Blutdruck, Blutzucker und Elektrolyten
- Verabreichung von Protonenpumpenhemmern (z.B. Omeprazol)
- Vor Therapiebeginn sollten folgende Untersuchungen durchgeführt werden:
Apheresetherapie:
Bei unzureichendem Effekt der Glucocorticoidtherapie (schwere, steroidrefraktäre Schubsymptomatik) sollte eine Apheresetherapie mittels Plasmapherese oder Immunadsorption erwogen werden.
Verlaufsmodifizierende Therapie
Allgemeines
- Grundprinzip: langfristige immunmodulatorische Stufentherapie
- Therapiebeginn:
- Frühzeitiger Beginn bei allen Patient:innen mit MS oder klinisch isoliertem Syndrom (KIS)
- Aufschieben des Therapiebeginns nur in Ausnahmefällen
- Ziele:
- Verringerung der Krankheitsaktivität
- Reduktion der Schubfrequenz
- Verzögerung der Krankheitsprogression
- Abnahme der Häufigkeit neuer MS-Läsionen im MRT
- Erhalt der Lebensqualität
- Die Wahl der immunmodulatorischen Therapie erfolgt nach:
- Krankheitsaktivität
- Verlaufsform
- Individuellen Faktoren (z.B. Begleiterkrankungen, Familienplanung)
MerkeIndividuelle Therapieplanung
Bei der Auswahl immunmodulatorischer Therapien sollten neben der antizipierten Wirksamkeit stets auch Aspekte der Sicherheit, potenzielle Neben- und Wechselwirkungen, bestehende Komorbiditäten sowie der Impfstatus und Fragen der Familienplanung berücksichtigt werden. Die endgültige Entscheidung sollte im Rahmen einer gemeinsamen, fundierten Nutzen-Risiko-Abwägung mit dem/der Patient:in erfolgen.
Übersicht der Wirkstoffe
Die derzeit verfügbaren Immuntherapien zur Behandlung der MS werden gemäß den aktuellen Leitlinien in drei Wirksamkeitskategorien eingeteilt. Diese Kategorisierung basiert auf der jeweiligen relativen Risikoreduktion der Schubrate. Eine höhere Wirksamkeit geht dabei häufig – wenn auch nicht zwingend – mit einem erhöhten Nebenwirkungsrisiko einher.
| Wirksamkeitskategorie 1 (mäßig wirksam) | Wirksamkeitskategorie 2 (stark wirksam) | Wirksamkeitskategorie 3 (höchst wirksam) |
|
|
|
Therapiealgorithmus nach Verlaufsform
Radiologisch isoliertes Syndrom (RIS):
- In der Regel Zuwarten unter regelmäßigen Verlaufskontrollen:
- Klinische und MRT-gestützte Verlaufskontrollen (Erstkontrolle nach 6 Monaten, anschließend alle 12 Monate)
- Bei Behandlungswunsch und bestehenden Risikofaktoren einer zeitnahen klinischen Manifestation (z.B. hohe Läsionslast im MRT) kann eine Off-label Therapie mit Teriflunomid oder Dimethylfumarat erwogen werden.
Klinisch isoliertes Syndrom (KIS/CIS):
- Bei Personen mit KIS sollte grundsätzlich eine immunmodulatorische Therapie begonnen werden
- Zugelassene Wirkstoffe: Interferon-ß-1a, Interferon-ß-1b
Schubförmig remittierende MS (RRMS):
- Beginn einer Immuntherapie grundsätzlich anzustreben
- Bei leichten Verlaufsformen der RRMS → Medikament aus der Wirksamkeitskategorie 1:
- Welche der 4 Substanzgruppen zum Einsatz kommt, sollte in Abhängigkeit von Nebenwirkungen, individuellen Präferenzen und Vorerkrankungen entschieden werden
- Zurückhaltender Einsatz von Teriflunomid bei Frauen mit Kinderwunsch (teratogenes Potential)
- Bei wahrscheinlich hochaktiven oder entzündlich-aktiven Verläufen → Medikament aus der Wirksamkeitskategorie 2 oder 3:
- Wie auch bei Substanzen der Kategorie 1 sollten bei der Wahl des Medikaments immer spezifische individuelle Aspekte berücksichtigt werden
- Empfehlungen zu Medikamenten der Wirksamkeitskategorie 3:
- Bestimmung des JCV-Antikörperstatus vor Therapiebeginn:
- Erhöhtes Risiko für PML unter Natalizumab
(insb. bei JCV-AK-positiven Personen) - Bei JCV-AK-seropositiven Patient:innen sollten CD20-Antikörper die Therapie der ersten Wahl sein
- Erhöhtes Risiko für PML unter Natalizumab
- Alemtuzumab
sollte nur zum Einsatz kommen, wenn eine Therapie mit Natalizumab oder CD20-Antikörpern nicht möglich ist
- Bestimmung des JCV-Antikörperstatus vor Therapiebeginn:
InfoPersonen mit unbehandelter RRMS soll eine Immuntherapie angeboten werden, wenn mind. ein klinisch objektivierbarer Schub oder MRT-Aktivität in einem Zeitraum von 2 vorausgegangenen Jahren nachweisbar war.
Primär progrediente MS (PPMS):
- Zur Behandlung der PPMS sollen ausschließlich CD20-Antikörper eingesetzt werden:
- Ocrelizumab: einziges zugelassenes Präparat bei PPMS
- Rituximab
(Off-Label)
- Strenge Indikationsstellung bei Patient:innen >50 Jahre
Sekundär progrediente MS (SPMS):
- Indikation für Immuntherapie nur bei aktiver SPMS (Nachweis von Schubaktivität oder neuen Läsionen im MRT)
- Zugelassene Wirkstoffe: Siponimod, Beta-Interferone
, Cladribin, Ponesimod und CD20-Antikörper
Symptomatische Therapie
Die symptombezogene Therapie bildet eine zentrale Säule des Behandlungskonzepts bei Multipler Sklerose und umfasst sowohl medikamentöse als auch nicht-medikamentöse Maßnahmen.
MS-assoziierte Symptome sollten regelmäßig erfasst werden. Bei nachgewiesener funktioneller Beeinträchtigung ist eine adäquate Therapie unter Berücksichtigung des individuellen Nebenwirkungsprofils einzuleiten.
Spastik
- Nicht-medikamentöse Maßnahmen: Physiotherapie (zentrales Behandlungselement!)
- Ggf. zusätzlich medikamentöse Maßnahmen:
- Mittel der 1. Wahl: Baclofen, Tizanidin
- Gabapentin: kann bei paroxysmaler Spastik
erwogen werden - Cannabinoide: möglicher Einsatz bei Unverträglichkeit oder mangelnder Wirksamkeit anderer Antispastika
- Invasive Verfahren:
- Indikation: unzureichendes Ansprechen oder nicht tolerable Nebenwirkungen der oralen bzw. oromukosalen Medikation
- Verfahren:
- Botulinumtoxin A (fokale Spastik
) - Baclofen intrathekal
- Botulinumtoxin A (fokale Spastik
Ataxie
- Nicht-medikamentöse Maßnahmen: Physio- und Ergotherapie
- Medikamentöse Maßnahmen (nur bei Tremor):
- Bei beeinträchtigendem Tremor kann der Einsatz von Propanolol, Primidon, Topiramat oder Levetiracetam erwogen werden
- Bei fortbestehender Therapieresistenz kann ein Versuch mit Botulinumtoxin erwogen werden
Fatigue:
- Nicht-medikamentöse Maßnahmen:
- Schulungen zum Energiemanagement
- Kognitive Verhaltenstherapie
- Achtsamkeits- und Aufmerksamkeitstraining
- Medikamentöse Therapie: Antidepressiva
(→ Einsatz nur bei gleichzeitig bestehender depressiver Verstimmung empfohlen)
Störungen der Sexualität:
- Nicht-medikamentöse Maßnahmen:
- Sexualtherapie
- Beckenbodentraining und ggf. transkutane Stimulation des N. tibialis (PTNS)
- Medikamentöse Maßnahmen:
- Erektile Dysfunktion: PDE-5-Hemmer (z.B. Sildenafil)
- Frauen mit verminderter Libido oder Dyspareunie: ggf. Einsatz von Hormonpräparaten (z.B. Tibolon)
Neurogene Dysfunktion des unteren Harntrakts:
- Nicht-medikamentöse Maßnahmen:
- Beckenbodentraining (mit oder ohne Elektrostimulation)
- Strukturierte urologische Rehabilitation
- Medikamentöse Maßnahmen:
- Neurogene Detrusor-Überaktivität: Anticholinergika
- Neurogene Detrusor-Unteraktivität: Alphablocker wie Tamsulosin (Off-Label)
- Nykturie
/Pollakisurie : Desmopressin
- Neurogene Detrusor-Überaktivität: Anticholinergika
Neurogene Darmfunktionsstörungen:
- Obstipation
: - Nicht-medikamentöse Maßnahmen:
- Ausreichende Flüssigkeitszufuhr und ballaststoffreiche Mischkost
- Körperliche Aktivität
und Physiotherapie - Bei fehlendem Effekt: transanale Irrigation
- Medikamentöse Maßnahmen:
- Bei hartem Stuhl: Lactulose
oder Macrogol - Zur Rektumentleerung: Glycerinzäpfchen, ggf. Klistiere
- Bei schmerzhafter Sphinkterspastik: Botulinumtoxin
- Bei starkem Meteorismus: Dimeticon
- Bei hartem Stuhl: Lactulose
- Nicht-medikamentöse Maßnahmen:
- Inkontinenz
: - Nicht-medikamentöse Maßnahmen:
- Individuelle Ernährungsumstellung
- Gezieltes regelmäßiges Abführen (z.B. durch transanale Irrigation)
- Ggf. Beckenbodentraining und/oder Elektrostimulation
- Ggf. adäquate Versorgung mit Hilfsmitteln (z.B. intraanale Tampons)
- Individuelle Ernährungsumstellung
- Medikamentöse Maßnahmen: ggf. Loperamid
oder Anticholinergika
- Nicht-medikamentöse Maßnahmen:
Prognose
Die Multiple Sklerose weist in der Regel einen chronisch-progredienten Verlauf auf, wobei das individuelle Fortschreiten stark variiert. Obwohl es bisher keine kausale Heilung gibt, hat sich die Prognose in den letzten 20 Jahren dank fortschrittlicher Diagnosetechniken und einer Vielzahl krankheitsmodifizierender Therapien deutlich verbessert.
Die Lebenserwartung von Patient:innen mit Multipler Sklerose liegt durchschnittlich etwa 5–10 Jahre unter der der Allgemeinbevölkerung. Hauptursachen hierfür sind ein erhöhtes Risiko für Infektionen, respiratorische Komplikationen sowie eine gesteigerte Suizidalität.
Quellen
- Grehl H, Reinhardt F: Checkliste Neurologie, Georg Thieme Verlag, 2022, ISBN: 9783132438088
- Hacke W: Neurologie, Springer Verlag, 2015, ISBN: 978-3662468913
- Faiss J: Multiple Sklerose, 2021, Urban & Fischer/Elsevier, ISBN: 9783437220852
- S2k-Leitlinie: Diagnose und Therapie der Multiplen Sklerose, Neuromyelitis-optica- Spektrum-Erkrankungen und MOG-IgG-assoziierten Erkrankungen, Deutsche Gesellschaft für Neurologie
- Montalban Xavier et al.: Diagnosis of multiple sclerosis: 2024 revisions of the McDonald criteria. The Lancet Neurology. 2025; 24(10):A-850-865. doi: 10.1016/s1474-4422(25)00270-4



